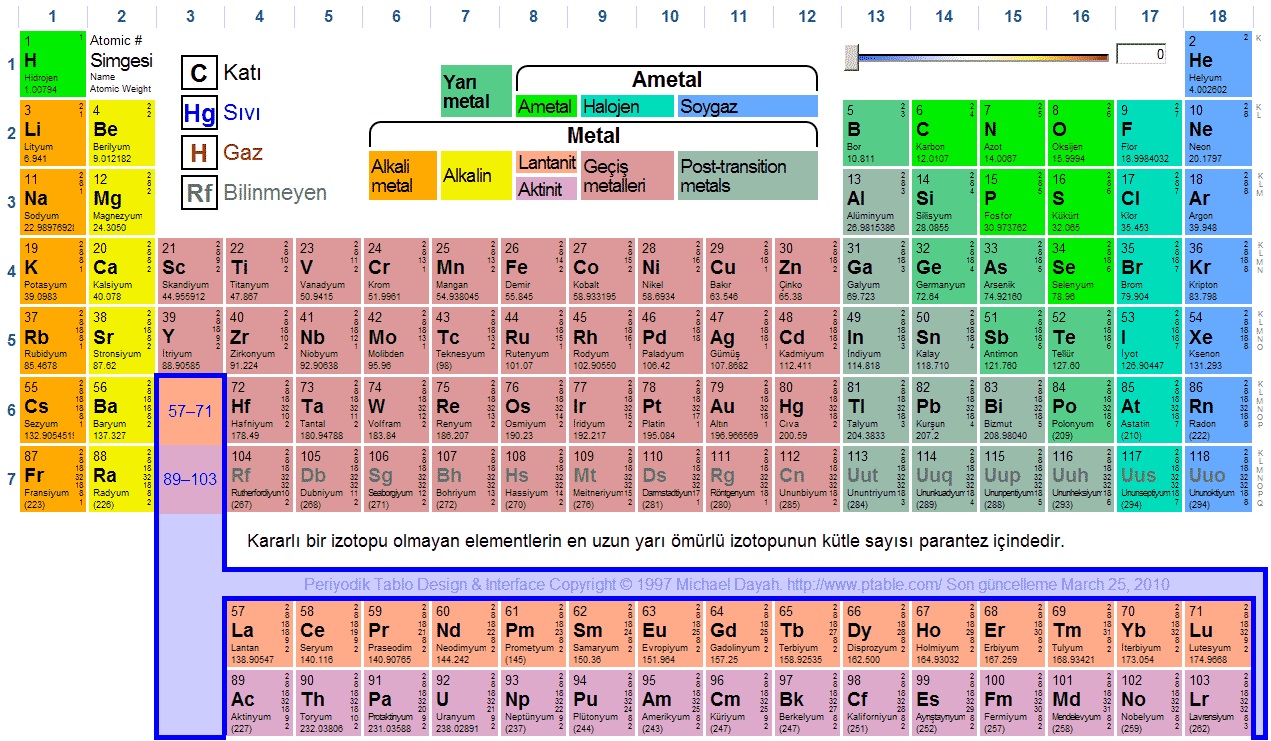
Periyodik Tablo Nedir?
Elementler, fiziksel ve kimyasal özellikler gösterirler. Elementlerden bazıları benzer özellikler gösterebilirken bazıları da farklı özellikler gösterirler. Bilim insanları elementler arasındaki ilişkileri bulmak için çeşitli çalışmalar yapmışlardır (1860’ların sonuna doğru). Dimitri Mendeleyev ve Meyer adlı iki bilim insanı birbirinden bağımsız olarak o güne kadar bulunmuş olan, bilinen 63 elementi sınıflandırmış ve aynı sıralamayı bulmuşlardır. Böylece elementler arasındaki ilişkiyi tablo haline getirmiş oldular. Henry Moseley ise bu elementleri atom numaralarına (proton sayılarına) göre sıralayarak periyodik tabloyu oluşturdu.
Periyodik Tablonun Tarihsel Gelişimi
1- Johann Wolfgank Döbereiner (Yohan Volfkank Döberaynar) – (1780 – 1849)
Benzer özellik gösteren elementleri üçerli gruplar hâlinde göstermiştir. Döbereiner’a göre lityum, sodyum ve potapotasyum benzer özellikler gösterdiği için aynı grupta yer almıştır.
2- Alexandre Beguyer de Chancourtois (Aleksandır Beguyer Dö Şankurtua) – (1820 – 1886)
Benzer özellik gösteren bazı element ve iyonları dikey bir sırada gösteren bir tablo oluşturmuştur.
3- John Newlands (Con Nivlinds) – (1837 – 1898)
Elementleri atom ağırlıklarına göre sıralamıştır. İlk sekiz elementten sonra benzer özelliklerin tekrar ettiğini keşfetmiştir. Oluşturduğu tabloyu müzikteki notalara benzetmiştir
4- Dimitri İvanovic Mendeleyev – (1834 – 1915)
5- Lothar Mayer – (1830 – 1895)
 Mendeleyev ve Mayer birbirinden habersiz aynı sıralamayı elde etmişlerdir. Mayer, elementleri benzer fiziksel özelliklerine göre sıralarken Mendeleyev, elementleri
Mendeleyev ve Mayer birbirinden habersiz aynı sıralamayı elde etmişlerdir. Mayer, elementleri benzer fiziksel özelliklerine göre sıralarken Mendeleyev, elementleri
atom ağırlıklarına göre sıralamıştır. Mendeleyev’in oluşturduğu tablo 12 satır ve 8 sütundan oluşmaktadır. Mendeleyev, günümüzde kullandığımız periyodik sisteme benzer bir sistem oluşturmuştur.
6- Henry Moseley (Henri Mozeli) – (1817 – 1915)
1913 yılında periyodik sistemi atom numaralarına göre düzenlemiştir.
7- Glenn Seaborg (Gilen Siborg) – (1912-1999)
Periyodik sistemin en altında yer alan
iki sıra hâlindeki elementleri düzenleyerek
günümüzdeki periyodik sisteme son
şeklini vermiştir.
Periyodik Tablonun Özellikleri
– Doğada 94 tane element bulunmaktadır. İnsanların laboratuarda elde ettiği yapay elementlerle bu sayı 120’ye yakındır.
– Periyodik tabloda elementler artan atom numaralarına göre sıralanırlar.
– Elementler sıralandığında oluşan tablodaki yatay sıralara periyot denir. Periyodik sistemde 7 periyot vardır.
– Periyodik tablodaki sütunlara grup denir. Gruplardaki elementler benzer kimyasal özelliklerine göre alt alta getirilerek sıralanmışlardır.Periyodik tabloda 8 tane A grubu, 8 tane B grubu (8B grubu 3 sütun) olmak üzere 18 grup vardır. Bu gruplardan bazıları özel olarak adlandırılmışlardır.
2A Grubu- Toprak Alkali Metaller
3A Grubu- Toprak Metalleri
7A Grubu- Halojenler
8A Grubu- Soygazlar
B Grubu Elementleri- Geçiş Metalleri
-1A Grubu (Hidrojen hariç), 2A Grubu, 3A Grubu (Bor hariç) ve 4A Grubundaki Kalay (Sn) ve Kurşun (Pb) metaldir. Ayrıca B Grubu Elementleri (Geçiş Metalleri) de metaldir.
-4A Grubundaki Karbon (C), 5A, 6A, 7A Grubu elementleri ametaldir.
-8A Grubu elementeri ise soygazlardır (asal gazlardır).
-3A Grubundan başlayıp 8A Grubuna doğru çapraz giden kısım ise yarı-metaldir. Bor (B), Silisyum (Si), Germanyum (Ge), Tellür (Te) yarı metal elementlerdendir.
Konu hakkında detaylı bilgi edinmek için aşağıdaki yazılarımızı inceleyebilirsiniz.
Maddenin Yapısı ve Özellikleri
Elementler ve Kullanım Alanları
Elementlerin Sınıflandırılması-Metaller, Ametaller, Yarı Metaller ve Soygazlar
Elementlerin Periyodik Tablodaki Yerinin Bulunması
Periyodik Cetvelin Özelliklerinin Değişimi
Kimyasal Bağ Nedir? Çeşitleri Nelerdir?
Bileşiklerin Adlandırılması ve Bileşiklerin Yapısındaki Atom Sayısının Bulunması
Asitler, Bazlar ve Tuzların Özellikleri